¿Qué son?
Los carbohidratos son los compuestos orgánicos más abundantes de la biósfera y a su vez los más diversos. Normalmente se los encuentra en las partes estructurales de los vegetales y también en los tejidos animales, como glucosa o glucógeno. Estos sirven como fuente de energía para todas las actividades celulares vitales.
También se les puede conocer por los siguientes nombres:
· Sacáridos (de la palabra latina que significa azúcar), aunque el azúcar común es uno solo de los centenares de compuestos distintos que pueden clasificarse en este grupo.
· Glícidos o glúcidos (de la palabra griega que significa dulce), pero son muy pocos los que tienen sabor dulce.
Composición
En su composición entran los elementos carbono, hidrógeno y oxígeno, con frecuencia en la proporción Cn(H20)n, por ejemplo, glucosa C6(H2O)6 de aquí los nombres carbohidratos o hidratos de carbono.
Estos compuestos, abarcan sustancias muy conocidas y al mismo tiempo, bastante disímiles, azúcar común, papel, madera, algodón, son carbohidratos o están presentes en ello en una alta proporción.
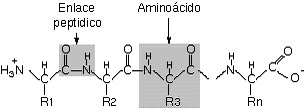
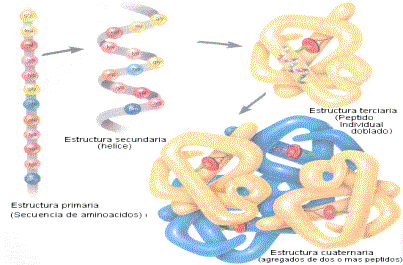
Estructura
Un aspecto importante de los hidratos de carbono es que pueden estar unidos covalentemente a otro tipo de moléculas, formando glicolípidos, glicoproteínas (cuando el componente proteico es mayoritario), proteoglicanos (cuando el componente glicídico es mayoritario) y peptidoglicanos (en la pared bacteriana).
En cuanto a sus propiedades fisicoquímicas, los carbohidratos de peso molecular bajo son solubles en agua y tienen poder edulcorante (endulzante) alto, características que son opuestas en los carbohidratos de peso molecular alto en los cuales la solubilidad se reduce notablemente.
Clasificación
Dependiendo de su composición, los carbohidratos pueden clasificarse en:
· monosacáridos: son azúcares simples, dulces y solubles en agua. Donde principalmente figuran las trisas, pentosas, hexosas (fructosa y galactosa) y la glucosa, que proporcionan energía de uso inmediato para las actividades celulares.
· oligosacáridos: son moléculas pequeñas que resultan por condensación o deshidratación de la unión de algunos monosacáridos, entre ellos figuran los di y trisacáridos. También son dulces y solubles en agua.
· polisacáridos: son polímeros que se forman con la unión de muchos monosacáridos; no son dulces si solubles en agua. Entre ellos figura la celulosa (constituyente de la pared celular), el almidon y glucógeno, que son reservas energéticas en células vegetales y animales.
Funciones principales.
- · Función energética. Cada gramo de carbohidratos aporta una energía de 4 Kcal. Ocupan el primer lugar en el requerimiento diario de nutrientes debido a que nos aportan el combustible necesario para realizar las funciones orgánicas, físicas y psicológicas de nuestro organismo.
- · Una vez ingeridos, los carbohidratos se hidrolizan a glucosa, la sustancia más simple. La glucosa es de suma importancia para el correcto funcionamiento del sistema nervioso central (SNC) Diariamente, nuestro cerebro consume más o menos 100 g. de glucosa, cuando estamos en ayuno, SNC recurre a los cuerpos cetónicos que existen en bajas concentraciones, es por eso que en condiciones de hipoglucemia podemos sentirnos mareados o cansados.
- · También ayudan al metabolismo de las grasas e impiden la oxidación de las proteínas. La fermentación de la lactosa ayuda a la proliferación de la flora bacteriana favorable
Enfermedades
¿QUÉ PASA CON EL EXCESO Y LA DEFICIENCIA DE LOS CARBOHIDRATOS?
El exceso de hidratos de carbono en la alimentación provoca: sobrepeso, obesidad y hasta diabetes.
La falta de carbohidratos causa: desnutrición, debilidad, irritabilidad, cansancio y falta de energía física y mental.
Para leer más:
¿Te da flojera leer? ¡Aquí un video!: